三氧化硫的原子间如何成键?
关注者
2被浏览
21,6602 个回答
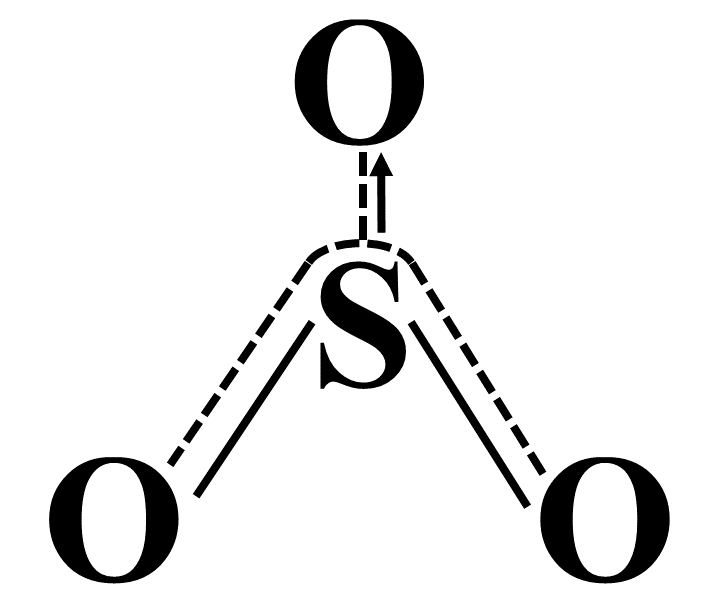
硫原子是中心原子,最外层有6个电子,采用sp^2杂化。两个sp^2杂化轨道填充1个电子,命名为sp^2_a 轨道和sp^2_b 轨道,另一个sp^2 杂化轨道填充2个电子,命名为sp^2_c 轨道,p_z 轨道上填充2个电子;
氧原子最外层有6个电子,亦均采用sp^2 杂化。2个氧原子分别命名为氧原子a和氧原子b,它们的核外电子排布方式相同,2个sp^2 轨道各填充2个电子,另一个sp^2 轨道填充1个电子,两个氧原子的这个sp^2 轨道分别命名为sp^2_a '和sp^2_b ',p_z轨道上填充1个电子;另一个氧原子命名为氧原子c,2个sp^2 轨道和p_z 轨道各填充2个电子,另一个sp^2 轨道不填充电子,命名为sp^2_c '轨道。
硫原子的sp^2_a 和sp^2_b 轨道分别与氧原子a和氧原子b的sp^2_a '和sp^2_b '轨道重合形成σ键,硫原子的sp^2_c轨道与氧原子c的sp^2_c '轨道重合形成配位σ键,4个原子的p_z 轨道共有6个电子,形成4中心6电子离域π键。
以上仅是猜想。


